Нітритна кислота: Формула, Властивості та Застосування
Нітритна кислота, формула якої є HNO2, є важливою хімічною сполукою в світі аналітичної та органічної хімії. Вона має цікаві фізико-хімічні властивості та знаходить застосування в різних галузях промисловості. У цій статті ми розглянемо формулу нітритної кислоти, характеристики, методи отримання та її використання.
Хімічні властивості нітритної кислоти: формула та структура
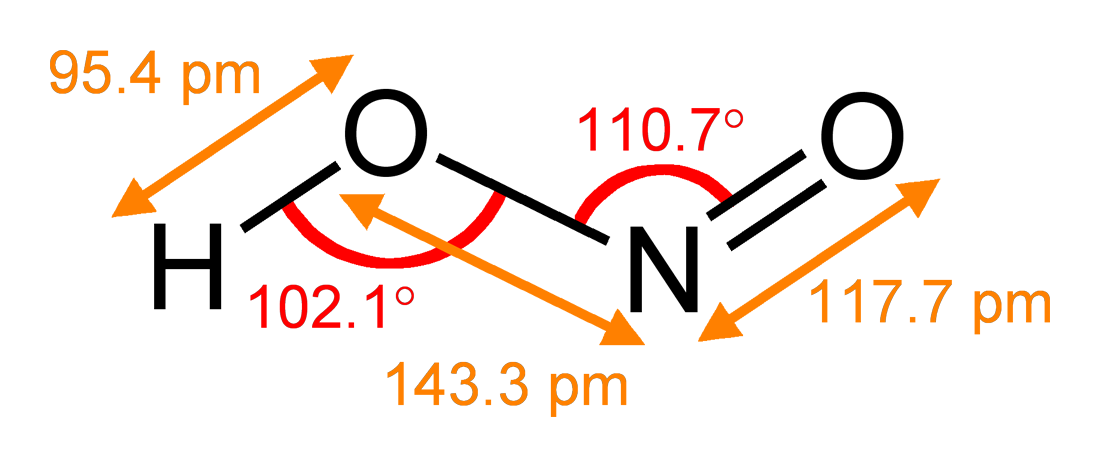
Нітритна кислота, формула якої HNO2, складається з одного атома водню (H), одного атома азоту (N) та двох атомів кисню (O). Основні характеристики цієї кислоти пояснюються її електронною структурою. Ось деякі важливі властивості нітритної кислоти:
- Молекулярна маса: 47.013 г/моль
- Стан: Зазвичай зустрічається у водному розчині, оскільки в чистій формі нестабільна.
- Розчинність: Добре розчиняється у воді.
- pKa: 3.35, що вказує на її помірну кислотність.
Отримання та хімічне поводження
У лабораторних умовах нітритну кислоту часто отримують шляхом реакції розведеної нітратної кислоти з металами, які утворюють нітрити, або через прямий синтез з оксиду азоту(III). HNO2 – слабка кислота, яка може існувати в рівновазі з газоподібним диоксидом азоту (NO2) в кислотних умовах. Формули, що характеризують згадані процеси, виглядають так:
- HNO3 + M → MNO2 + H2O
- NO + NO2 + H2O → 2 HNO2
Застосування нітритної кислоти
Нітритна кислота має кілька важливих застосувань у різних галузях, завдяки своїм відновлювальним та окислювальним властивостям:
| Галузь | Застосування |
|---|---|
| Аналітична хімія | Використовується для виявлення іонів заліза(II) та інших металів. |
| Органічна хімія | Служить проміжною ланкою у синтезі діазо-з’єднань, які є важливими компонентами фарб і пігментів. |
| Індустрія | Використовується як інгібітор корозії та для очищення стічних вод. |
Вплив на здоров’я та довкілля
Нітритна кислота, формула якої слабка, але здатна до утворення токсичних оксидів азоту за певних умов, потребує обережного поводження. Ось кілька важливих аспектів:
- Токсичність: Вплив парів нітритної кислоти може викликати подразнення дихальних шляхів, а прямий контакт з розчином – хімічні опіки.
- Екологічний вплив: Потенційно може спричинити окислення шкідливих сполук у ґрунті та водних об’єктах, але в надмірних кількостях може також призводити до забруднення навколишнього середовища.
Висновки
Отже, нітритна кислота, формула якої HNO2, є важливою хімічною сполукою з широким спектром застосувань у різних галузях науки та промисловості. Її широкий спектр властивостей дозволяє використовувати нітритну кислоту в аналітичних методах, органічному синтезі та індустрії. Проте, слід наголошувати на дотриманні запобіжних заходів під час роботи з цією речовиною, щоб уникнути потенційно небезпечних наслідків для здоров’я людини та довкілля.