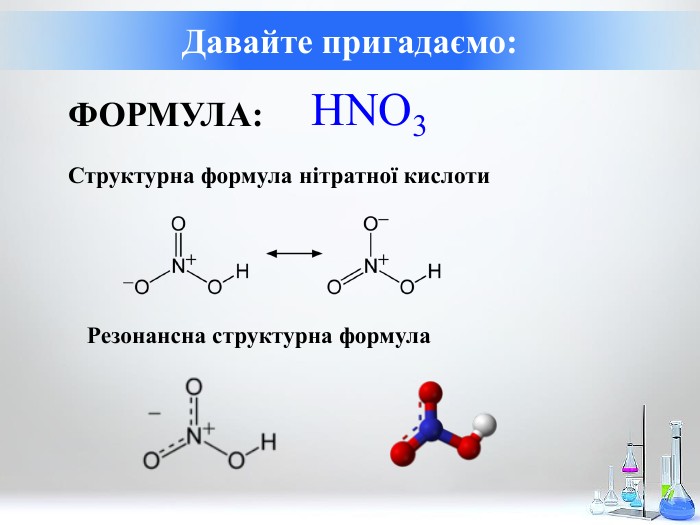
Формула нітратної кислоти: особливості та властивості
Формула нітратної кислоти — це HNO3, і вона є однією з найважливіших сполук в хімії, широко використовуючись у промисловості та медичних дослідженнях. Нітратна кислота є сильною неорганічною кислотою, відомою своїми окиснювальними властивостями та застосуванням у різних процесах. У цій статті ми розглянемо детально формулу нітратної кислоти, її властивості та взаємодію з металами.
Молекулярна структура та властивості
- Молекулярна формула: HNO3
- Молярна маса: приблизно 63,01 г/моль
- Фізичні властивості: Нітратна кислота є безбарвною рідиною, яка при тривалому зберіганні набуває жовтуватого відтінку через розпад і утворення оксидів азоту.
- Хімічні властивості: Це сильна кислота з високими окиснювальними властивостями. Реагує з більшістю металів, утворюючи нітрати.
Отримання та застосування
Нітратна кислота зазвичай отримується шляхом реакції окислення аміаку або через взаємодію азоту з водою. Найпоширенішим методом в промисловості є окиснення аміаку через процес Оствальда.
Основні області застосування нітратної кислоти включають:
- Виробництво добрив, таких як аміачна селітра.
- У хімічній промисловості для виробництва вибухових речовин, таких як нітрогліцерин і тротил.
- У металургії для травлення і очищення металів.
- У лабораторній практиці як реактив для аналізу.
Взаємодія з металами
Нітратна кислота реагує з металами з утворенням нітратів. Особливістю цієї взаємодії є те, що в залежності від концентрації кислоти та реактивності металу, в процесі можуть утворюватися різні гази, серед яких:
- Оксиди азоту: виділяються в разі реакції з більшістю металів.
- Водень: зазвичай не виділяється, бо нітратна кислота розкладає його на воду та оксиди азоту.
Нижче представлена таблиця з прикладами реакцій нітратної кислоти з деякими металами:
| Метал | Концентрація HNO3 | Продукти реакції |
|---|---|---|
| Мідь (Cu) | розведена | Cu(NO3)2, NO, H2O |
| Мідь (Cu) | концентрована | Cu(NO3)2, NO2, H2O |
| Алюміній (Al) | будь-яка | Al(NO3)3, N2O, H2O |
Заключення
Формула нітратної кислоти HNO3 відіграє важливу роль у сучасній хімії через свою широко застосування та унікальні властивості. Взаємодії цієї кислоти з металами відкривають широкі можливості для її використання у промисловості та наукових дослідженнях. Знання про хімічні реакції нітратної кислоти допомагають краще зрозуміти процеси, що відбуваються в хімічній промисловості, та забезпечують безпечне її використання.